北海道大学は、精神的ストレスによる脳腸相関のメカニズムの一端を解明したと発表した。
自然免疫や腸内細菌との共生をになっている小腸の細胞が分泌する作用因子が、心理的ストレスによって減少することを明らかにした。
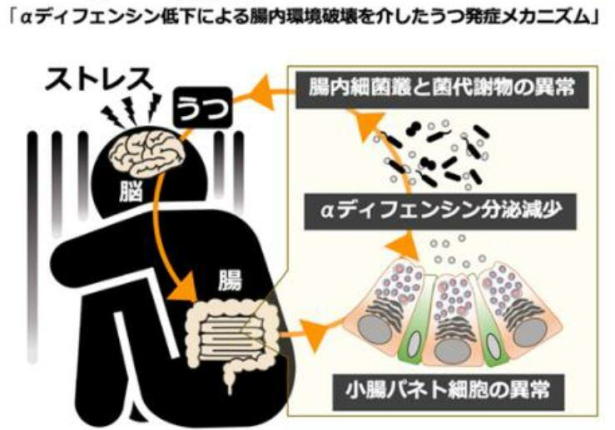
この作用因子は、うつ状態を起こすようなストレスにさらされると減少し、腸内細菌叢と腸内代謝物に異常をもたらし、腸内環境の恒常性が乱れるという。
心理ストレスによるうつ病に腸内細菌叢が大きく関わっている
腸内には多くの数と種類の細菌が常在しており、その集団は「腸内細菌叢」と呼ばれる。細菌の組成や腸内細菌叢としての多様性が変化することが、肥満や2型糖尿病などの生活習慣病や、免疫アレルギー疾患、自閉症などの神経疾患、大腸がんなど、さまざまな疾患に影響すると考えられている。
腸内細菌叢と腸内代謝物の異常が、うつ病を発症させる心理的ストレスで生じることが、これまでの研究で示されている。しかし、なぜ心理的ストレスにより、腸内細菌叢の破綻が起こるのかはよく分かっていない。
うつ病は、抑うつ気分を特徴としており、意欲の低下や睡眠障害、倦怠感など、さまざまな心と体の不調をきたすことから、診断が難しいことが知られている。
一方、「脳腸相関」は、脳と腸は密接に関連しており、それらに双方向性の関係性があるという考え方。脳と腸は、自律神経系や副腎皮質刺激ホルモン放出因子をはじめとする、さまざまなホルモンなどを介してつながっている。最近は脳の機能に腸内細菌叢が関与していることが注目されている。
免疫や腸内細菌との共生をになっている作用因子を解明
小腸には、自然免疫や腸内細菌との共生をになっている「パネート細胞」と呼ばれる細胞がある。この細胞は、自然免疫ではたらく主要な作用因子である「αディフェンシン」という抗菌ペプチドを小腸内腔に分泌し、自然免疫や腸内細菌との共生をになっている。
αディフェンシンは、腸内細菌叢とその代謝物を調節することで、腸管の恒常性を維持する働きをしている。研究グループはこれまで、αディフェンシンが、腸内に常在している共生菌を殺さないで、選択的な殺菌活性により、腸内細菌叢の組成を適切にコントロールしていることを明らかにしてきた。
研究グループは今回の研究で、うつ病での脳腸相関に着目し、心理的ストレスにより、小腸のパネート細胞からのαディフェンシン分泌量が減少することをはじめて明らかにした。これにより腸内細菌叢とその代謝物の恒常性が乱れると考えられる。
研究は、北海道大学大学院先端生命科学研究院の中村公則准教授、綾部時芳教授らの研究グループによるもの。研究成果は、「Scientific Reports」にオンライン掲載された。
出典:北海道大学、2021年
心理的ストレスが腸内細菌叢を乱すメカニズムを明らかに
研究グループは今回、うつ病に関わる腸内細菌叢や腸内代謝物の恒常性の破綻と、αディフェンシンの関連性を明らかにするため、心理的ストレスに起因するうつ病モデルである慢性社会的敗北ストレスモデルマウスを用いて実験した。
これまで、うつ病でなぜ腸内細菌叢と代謝物に異常が起こるのかはよく分かっていなかったが、ストレスで起こるαディフェンシンという腸内自然免疫の機能低下が引き金となって、腸内細菌叢が異常になり、さらには腸内代謝物の恒常性が崩れるという一連の脳腸相関を、世界ではじめて明らかにした。
また、うつ病発症の早期の段階でも、心理ストレスにより、小腸のパネート細胞からのαディフェンシン分泌量が低下することも分かった。
「行動の変容を含めた全身的な影響については今後の検討が必要ですが、うつ病での腸のαディフェンシンと腸内細菌叢の関係性をさらに追求していくことで、将来的にうつ病に対して、脳腸相関という視点からの予防法や新規治療法を開発できる可能性があります」と、研究グループは述べている。
北海道大学大学院先端生命科学研究院
Decrease of α-defensin impairs intestinal metabolite homeostasis via dysbiosis in mouse chronic social defeat stress model(Scientific Reports 2021年5月10 日)




